

کیت TIBC آدیت | کیت بیوشیمی AUDIT TIBC | تعیین ظرفیت اتصال آهن کل
447,700 تومان قیمت اصلی: 447,700 تومان بود.430,000 تومانقیمت فعلی: 430,000 تومان.
جهت تشخیص و درمان کم خونی فقر آهن و سایر اختلالات متابولیسم آهن و تعیین ظرفیت اتصال آهن از کیت بیوشیمی AUDIT TIBC اسفاده می گردد.
خرید کیت TIBC آدیت را فقط از تستا انجام دهید.
معرفی کیت بیوشیمی AUDIT TIBC
Total iron-binding capacity (TIBC)
خرید کیت TIBC آدیت
کاربرد: برای استفاده در تعیین ظرفیت کل اتصال آهن در سرم روی آنالایزرهای شیمی خودکار کاربرد دارد.
تستا عرضه کننده کیت بیوشیمی AUDIT TIBC جهت تعیین ظرفیت اتصال آهن کل
برند: دلتا درمان پارت (آدیت)
محتویات: معرف های R1 و R2 و دستورالعمل استفاده
قیمت با ۴٪ تخفیف : ۴۳۰۰۰۰ تومان
فهرست مطالب
شرکت توسعه سلامت توان آفرین (تستا)، کیت بیوشیمی AUDIT TIBC جهت تعیین ظرفیت اتصال آهن کل عرضه می کند.
برای خرید کیت TIBC آدیت در تستا شاپ ثبت سفارش نمایید.
ویدیو معرفی کیت TIBC آدیت (کیت تعیین ظرفیت اتصال آهن کل)
تعیین ظرفیت اتصال آهن کل
Total iron-binding capacity (TIBC)
خلاصه ای از اصل آزمون و ارتباط بالینی
مقدمه
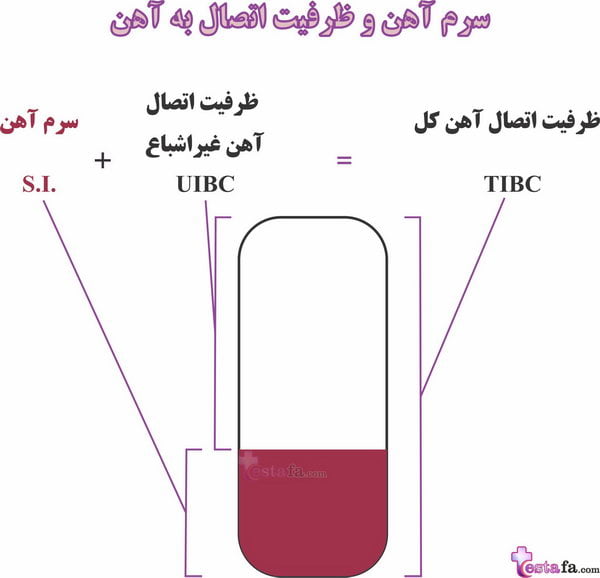
ظرفیت اتصال کل آهن (TIBC) به صورت غیر مستقیم به روش ظرفیت اتصال آهن غیراشباع (UIBC) انجام می شود.
یک استاندارد شناخته شده آهن ۱۰۵ میکرومول در لیتر (۵۸۶ میکروگرم در دسی لیتر) که با سرم در pH 7.9 انکوبه شده است، محل های اتصال موجود در ترانسفرین سرم را اشباع می کند. سپس آهن اضافی متصل نشده با فرن کمپلکس می شود تا فرن آهنی، یک کمپلکس آبی، که توسط سیستم LX اندازه گیری می شود، تشکیل شود. UIBC برابر است با کل آهن اضافه شده کمتر از آهن اضافی.
در سال ۱۹۷۰، استوکی سنتز فروزین را گزارش کرد که با آهن کمپلکس می شود و یک کمپلکس تریس فروزین/آهن، Fe(Fz)3 را تشکیل می دهد. مزایای عمده فروزین جذب مولی بالای کمپلکس فروزین (۲۸۰۰۰)، حلالیت در آب و پایداری آن در محدوده pH 4-9 است.
این آزمایش از یک ترکیب نوع فروئین، Ferene استفاده می کند. این معرف یک عامل کلات کننده آهن برتر است که یک کمپلکس فرن با آهن را با حداکثر جذب در ۵۹۳ نانومتر و جذب مولی ۳۵۵۰۰ تشکیل می دهد. LX20 از طول موج های تحلیلی ۶۰۰ نانومتر استفاده می کند. این ترکیب ۲۷ درصد جذب مولی بالاتری نسبت به فروزین دارد، در طول موج طولانی تری جذب می شود و مزایای دیگر فروزین یعنی حلالیت و پایداری آن را دارد.
اندازه گیری (UIBC) همراه با اندازه گیری آهن سرم در تشخیص و درمان هموکروماتوز ارثی و سایر اختلالات آهن استفاده می شود. مقدار ترکیبی UIBC و آهن سرم مقداری برای TIBC می دهد. این نشان دهنده حداکثر غلظت آهنی است که پروتئین های سرم می توانند به آن متصل شوند.
TIBC در کمبود آهن افزایش می یابد. حساسیت TIBC برای کمبود آهن کمتر از فریتین سرم است. TIBC در کم خونی بیماری مزمن کم است. TIBC پایین با فریتین و پارامترهای خونی تفسیر می شود.
روش اندازه گیری غلظت آهن
روش مورد استفاده برای اندازه گیری غلظت آهن یک روش نقطه پایانی زمان بندی شده است. در این واکنش، آهن توسط اسید استیک از ترانسفرین آزاد می شود و توسط هیدروکسیل آمین به حالت آهنی تبدیل می شود.
تیوگلیکولات یون آهن بلافاصله با معرف آهن فروزین کمپلکس می شود. این سیستم تغییر جذب را در ۵۶۰ نانومتر در یک بازه زمانی ثابت نظارت می کند. این تغییر در جذب مستقیماً با غلظت آهن در نمونه متناسب است.
اندازه گیری آهن سرم در ارتباط با ظرفیت اتصال کل آهن در تشخیص و درمان اختلالات مربوط به مکانیسم های دریافت، جذب، ذخیره و آزادسازی آهن مفید است. چنین تغییراتی نشان دهنده طیف گسترده ای از اختلالات از جمله کم خونی، نفروز، سیروز و هپاتیت است.
موارد استفاده مصرف
برای استفاده در تعیین ظرفیت کل اتصال آهن در سرم روی آنالایزرهای شیمی خودکار. فقط برای استفاده تشخیصی آزمایشگاهی.
ظرفیت اتصال کل آهن (TIBC) اندازه گیری توانایی پروتئین های سرم، عمدتا ترانسفرین، برای اتصال آهن است. حداکثر غلظت آهنی است که پروتئین های سرم می توانند به آن متصل شوند. همراه با غلظت کل آهن سرم، TIBC در تشخیص و درمان کم خونی فقر آهن، سایر اختلالات متابولیسم آهن و اختلالات التهابی مزمن استفاده می شود. به عنوان شاخصی از وضعیت تغذیه، TIBC سرم در کمبود آهن افزایش یافته و در کم خونی ناشی از بیماری مزمن کاهش می یابد.
همراه با آهن سرم و درصد اشباع ترانسفرین، پزشکان معمولاً این آزمایش را زمانی انجام می دهند که نگران کم خونی، فقر آهن یا کم خونی فقر آهن هستند. با این حال، از آنجا که کبد ترانسفرین تولید می کند، تغییرات در عملکرد (مانند سیروز، هپاتیت یا نارسایی کبد) باید در هنگام انجام این آزمایش در نظر گرفته شود. همچنین می تواند یک آزمایش غیر مستقیم برای عملکرد کبد باشد، اما به ندرت برای این منظور استفاده می شود.
درصد اشباع ترانسفرین (یعنی نتیجه فرمول آهن سرم/TIBC x 100) نیز می تواند یک شاخص مفید باشد. مطالعات همچنین نشان داد که اشباع ترانسفرین (غلظت آهن سرم ÷ ظرفیت اتصال کل آهن) بیش از ۶۰ درصد در مردان و بیش از ۵۰ درصد در زنان وجود یک ناهنجاری در متابولیسم آهن (هموکروماتوز ارثی، هتروزیگوت ها و هموزیگوت ها) را با دقت تقریباً ۹۵ درصد شناسایی کرد. . این یافته به تشخیص زودهنگام هموکروماتوز ارثی کمک می کند، به ویژه در حالی که فریتین سرم هنوز پایین است.
آهن باقیمانده در هموکروماتوز ارثی عمدتاً در سلولهای پارانشیم رسوب میکند و تجمع سلولهای رتیکولواندوتلیال در اواخر بیماری رخ میدهد. این برخلاف اضافه بار آهن تزریقی است که در آن رسوب آهن ابتدا در سلول های رتیکولواندوتلیال و سپس در سلول های پارانشیمی رخ می دهد. این توضیح می دهد که چرا سطح فریتین در هموکروماتوز ارثی نسبتا پایین باقی می ماند، در حالی که اشباع ترانسفرین بالا است.
نتایج غیر طبیعی TIBC
مقادیر بالا: TIBC زمانی که منابع آهن بدن کم باشد، نتیجه تست TIBC بالاتر از حد طبیعی است. این می تواند در یکی از شرایط ریز رخ دهد:
- کم خونی فقر آهن.
- کم خونی فقر اهن یا اواخر بارداری است.
- ناشی از مصرف داروهای ضد بارداری خوراکی.
مقادیر پایین: اگز نتیجه تست TIBC پایین تر از حد طبیعی باشد، ممکن است ناشی از موارد زیر باشد:
- کم خونی ناشی از سلول های قرمز خون که خیلی سریع نابود می شوند (کم خونی همولیتیک).
- سطح پروتئین پایین تر از حد طبیعی در خون (هیپوپروتئینمی).
- التهاب.
- بیماری کبد مانند سیروز.
روش انجام آزمون
مرحله ۱: اتصال آهن به رنگ
معرف ۱ (R1) ، یک بافر اسیدی حاوی رنگ اتصال آهن و کلرید آهن (III) به نمونه سرم اضافه می شود. pH پایین R1 آهن را از ترانسفرین آزاد می کند. سپس آهن با رنگ بافر اسیدی یک کمپلکس رنگی تشکیل می دهد. کمپلکس رنگی در پایان این مرحله اول، هم آهن سرمی و هم آهن اضافی موجود در R1 را نشان می دهد.
مرحله ۲: اتصال آهن به ترانسفرین
معرف ۲ (R2) ، سپس یک بافر خنثی اضافه می شود که pH را تغییر می دهد و در نتیجه میل ترکیبی ترانسفرین برای آهن افزایش می یابد. ترانسفرین سرم با انتزاع آهن از کمپلکس رنگ-آهن به سرعت به آهن متصل می شود.
کاهش مشاهده شده در جذب کمپلکس رنگی-آهن به طور مستقیم با ظرفیت کل اتصال آهن نمونه سرم متناسب است.
معرف ها
معرف ۱ (R1) حاوی ۱۶۶ مول در لیتر کرومازورول B، ۷۳۵ مول در لیتر ستریمید، ۱۶ میکرومول در لیتر کلرید آهن، بافر استات، تثبیت کننده ها و مواد نگهدارنده است.
معرف ۲ (R2) حاوی: ۳۳۸ میلی مول در لیتر بی کربنات سدیم، بافر، تثبیت کننده ها و نگهدارنده ها
آماده سازی معرف
معرف های مستقیم TIBC، R1 و R2 همانطور که عرضه می شوند آماده استفاده هستند.
شرایط نگهداری و پایداری معرف
معرف تا تاریخ انقضای نشان داده شده روی برچسب زمانی که در دمای ۸-۲ درجه سانتیگراد نگهداری شود پایدار است.
موارد احتیاط
کیت Direct TIBC برای استفاده تشخیصی آزمایشگاهی است. اقدامات احتیاطی معمولی برای دست زدن به معرف های آزمایشگاهی باید انجام شود.
- معرف را مصرف نکنید و از طریق دهان پیپت نکنید.
- از تماس با پوست و چشم جلوگیری کنید.
- معرف های با شماره های مختلف را مخلوط نکنید
تمام نمونه ها و کنترل های مورد آزمایش باید به طور بالقوه عفونی در نظر گرفته شوند. اقدامات احتیاطی همگانی، همانطور که در مورد تاسیسات شما اعمال می شود، باید برای جابجایی و دفع مواد در حین و بعد از آزمایش استفاده شود.
ذخیره سازی و جمع آوری نمونه
- سرم تازه و همولیز نشده نمونه انتخابی است. از پلاسما استفاده نکنید.
- نمونه ها باید از گلبول های قرمز جدا شده و به سرعت آنالیز شوند. با این حال، سرم ممکن است در دمای ۲ تا ۸ درجه سانتیگراد یا ۲۰- درجه سانتیگراد تا یک ماه نگهداری شود. سرم را می توان در دمای اتاق (۲۲-۲۸ درجه سانتیگراد) به مدت دو هفته نگهداری کرد.
مواد مورد نیاز اما ارائه نشده است:
- تجهیزات آزمایشگاهی عمومی
- ست کالیبراتور مستقیم TIBC
- کالیبراتور
کالیبراتور C.F.A.S-SP برای کالیبراسیون مورد نیاز است. برای دستورالعمل ها به درج بسته کالیبراتور مراجعه کنید. دستورالعمل های سازنده ابزار را برای عملکرد و فرکانس کالیبراسیون، با استفاده از نمونه های کنترل کیفیت در هر بار اجرا برای تأیید کالیبراسیون رضایت بخش، دنبال کنید. (نتایج بیان شده بر حسب µg/dL ممکن است با ضرب در ۰.۱۷۹۱ به µmol/L تبدیل شود.)
روش کار خودکار برای آنالایزرهای هیتاچی
۶۶۰ nm | Wavelength |
۳۷ °C | Temperature |
Endpoint | Mode |
۵ min | Reaction time step 1 |
۱۰ min | Reaction time step 2 |
۲۵ µL | Sample volume |
۲۵۰ µL | Reagent 1 (R1) volume |
۷۵ µL | Reagent 2 (R2) volume |
سنجش را می توان در انواع آنالایزرهای شیمی اتوماتیک انجام داد. جزئیات در صورت درخواست در دسترس است.
تمام داده های عملکرد موجود در اینجا با استفاده از تحلیلگر Roche Hitachi 911 به دست آمده است.
محاسبه نتایج
ابزار به طور خودکار نتایج را محاسبه می کند.
کنترل کیفیت
قابلیت اطمینان نتایج آزمایش باید با گنجاندن سرمهای کنترل با غلظتهای شناخته شده TIBC در هر آزمایش کنترل شود. این کنترل ها باید در طول فرآیند انجام شوند و به همان روشی که نمونه های سرم بیمار درمان می شوند، انجام شوند. بازیابی مقادیر کنترل در محدوده قابل قبول تعیین شده باید معیارهای مورد استفاده در ارزیابی عملکرد سنجش باشد.
خطی بودن
روش TIBC مستقیم خطی بودن بین ۷۷ و ۶۹۴ µg/dL TIBC را نشان داد.
دقت
سرم Accurar65 با غلظت TIBC در محدوده ۱۵۰-۵۵۰ µgliL با روش TIBC مستقیم و یک روش تجاری مبتنی بر جداسازی مغناطیسی TIBC مورد سنجش قرار گرفت.
تجزیه و تحلیل رگرسیون نتایج حاصل شد :
y = 1.02 (x) + 11.3, که در آن
Y= روش TIBC مستقیم در هیتاچی ۹۱۱
و X=
DTIBC روی کوباس فارا، و ضریب همبستگی (r) 0.991.
صحت
دو سطح TIBC با استفاده از مواد کنترل کیفیت Multiqual مورد آزمایش قرار گرفت. مطالعات دقت درون اجرا و دویدن به اجرا (هفت روز) نتایج زیر را به همراه داشت:
Within-Run Precision (N = 25)
Level 2 | Level 1 | |
۳۶۱ | ۲۱۶ | Mean (µg/dL) |
۳.۹ | ۶.۰ | S.D. (µg/dL) |
۱.۱ | ۲.۸ | C.V. (%) |
Run-to-Run (N = 25)
Level 2 | Level 1 | |
۳۶۲ | ۲۰۸ | Mean (µg/dL) |
۵.۷ | ۵.۲ | S.D. (µg/dL) |
۱.۶ | ۲.۵ | C.V. (%) |
نتایج مورد انتظار
۲۵۰ – ۴۵۰ µg/dL
از آنجایی که این محدوده ها با جمعیت های مختلف متفاوت است، توصیه می شود که هر آزمایشگاه محدوده مورد انتظار خود را تعیین کند.
محدودیت ها
- با استفاده از سرم های معمولی (متوسط TIBC: تقریباً ۳۵۰ میکروگرم در دسی لیتر)، مواد زیر برای تداخل احتمالی با افزودن آزمایش شدند و حداقل محدودیت های داده شده کمتر از ۵ درصد سوگیری را نشان دادند:
- بیلی روبین تا ۲۵.۶ میلی گرم در دسی لیتر
- هموگلوبین تا ۵۰۰ میلی گرم در دسی لیتر
- تری گلیسیرید تا ۱۶۹۰ میلی گرم در دسی لیتر
- مس تا ۳ میلی گرم در دسی لیتر
- روی تا ۲۵۰ µg/dL
- نیکل تا ۵۰۰ µg/dL
- Cuprimine تا ۲۵۰ µg/dL
- ایمفرون (به عنوان آهن) تا ۱۴۳۰ µg/dL
- آسکوربات بیش از ۲۰ میلی گرم در دسی لیتر اسید اسکوربیک باعث کاهش قابل توجه نتایج TIBC می شود.
- دسفرال کمتر از ۵% بایاس تا ۱۱.۵ µg/mL و کمتر از ۱۰% بایاس تا حداقل ۲۳ µg/mL نشان داد.
- سرم نمونه ارجح است، از پلاسما استفاده نکنید.
جهت تعیین ظرفیت اتصال آهن استفاده از کیت TIBC آدیت توصیه می گردد.
تستا عرضه کننده انواع کیت های آزمایشگاهی و لوازم مصرفی آزمایشگاهی و کیت بیوشیمی AUDIT TIBC
NCCLS. Determination of Serum Iron and Total Iron Binding Capacity; Proposed Standard. NCCLS Document H17-P. Wayne, PA: NCCLS, Vol. 10, No. 4; 1990. https://clsi.org/media/1347/c61a_sample.pdf
Starr RT. Use of an Alumina Column in Estimating Total Iron-Binding Capacity. Clin. Chem. 26: 156-158, 1980. https://manualzz.com/doc/5168449/feuillet-technique-tibc---laboratoire-de-biologie-m%C3%A9dical...








دیدگاهها
هیچ دیدگاهی برای این محصول نوشته نشده است.